코로나 바이러스 감염증의 출현 후, 항 바이러스와 항균에 대한 관심이 크게 높아지면서 이와 관련된 제품이 하나 둘 나온다.
최근까지는 크게 중요하고 다루지 못한 항 바이러스 및 항균 평가가 현재는 업태와 관계 없이 필수적인 분석으로 텔레비전 광고에 지표로 나타나고 있다.
다양한 바이러스, 세균에 의한 병의 위험에 의해서 항 바이러스성, 항균 능력의 중요성이 각인된 만큼 구매자도 항 바이러스 및 항균 능력을 가진 제품을 선호하고 있다.
그러므로 향후는 항 바이러스성 및 항균 능력을 가진 제품의 평가가 필수 아니면 안 되고 분석 결과를 토대로 지속적인 품질 개선이 이루어져야 할 것이다.
바이러스와 세균의 차이
바이러스와 세균

바이러스와 세균은 크기부터가 다르다.
바이러스의 크기는 30~300nm(나노 미터)로 세균의 크기는 1~5μm(마이크로 미터)에서 바이러스가 세균보다 훨씬 작다.
또 바이러스와 세균은 구조에서도 차이가 있다.
세균은 하나의 독립된 세포로 이루어진 생물체에서 세포막과 세포 벽, 세포 벽, 핵, 단백질 등으로 구성된 반면, 바이러스는 단백질과 핵산(DNA나 RNA)에서 되는 생물과 무생물의 중간 형태로 보다 단순한 구조를 갖는다.
가장 큰 특징은 바이러스는 혼자서 증식하지 못하고 숙주 세포가 존재해야 생장이 가능하다는 특징이 있다.
세균과 바이러스는 병원체가 됐을 때의 대처 법도 다르다.
세균의 경우에는 그 세포 벽을 약하게 만들고 감염된 세포를 죽이는 항생제로 치료를 하고, 바이러스의 경우는 백신이나 항 바이러스제를 이용한다.
백신은 바이러스를 약하게 만들거나 죽여서 체내에 미량을 주입한 것이며, 항 바이러스제는 몸에 침입한 바이러스의 증식을 억제하거나 바이러스 자체를 없애는 것이다.
항 바이러스 능력을 평가할 때 전제하지 않으면 안 되는 것이 바로 바이러스의 다양한 변종에 대한 모니터링을 할 수 없다는 뜻이다.
바이러스는 구조상 수시로 변종을 만들고 각각의 특성도 변화가 있어 어떤 물질과 기능이 특정 바이러스에 항 바이러스성을 갖는다는 것이 모든 바이러스에 공통으로 적용되는 것은 아니다.
이 때문에 물질의 기능과 특성에 항균 능력이 고려될 수밖에 없다.
항균 능력은 정확하게 생명체로 기능하는 미생물에 대한 영역이기 때문에 항균 능력을 갖는다는 것은 무한대의 바이러스에 대해서도 강력한 저항력을 가지는 것을 의미한다.
항균 능력 평가 및 항 바이러스성 평가

항균성 평가

1. 디스크 검사법 : : Paper disc method

디스크 확산법은 세균의 항균물질 감수성을 측정하는 방법이다.
항균물질이 포함된 디스크를 배지에 얹으면 디스크 주변에 항균물질 성분이 농도 구배를 형성하면서 확산된다.
세균이 항균물질에 대한 감수성을 가질 경우 항균물질 성분이 특정 농도 이상인 부분에서 세균의 생장이 억제돼 고리형 억제 영역을 관찰할 수 있다.
이 억제 영역의 직경을 측정해 세균이 항균 물질에 어느 정도 감수성을 갖는지 판별할 수 있다.
이 방법은 적은 비용으로 다양한 종류의 항균물질에 대한 세균의 감수성을 확인할 수 있는 장점이 있다.
2. 최소억제농도(MIC)희석 법의 장점은 정량적인 결과인 최소 억제 농도(minimum in hibitory concentration, MIC)을 얻게 되고, 디스크 확산 법에서 검사할 수 없는 세균의 감수성 결과를 정확히 얻을 수 있다는 것이다.
액체 배지 시험관 희석 법(broth macrodilution)과 액체 배지 미량 희석 법(broth microdilution)이 있으며 최근에는 상품화된 후자의 방법이 널리 쓰인다.
액체 배지 시험관 희석 법은 널리 사용되지 않지만, 최소 살균 농도(minimum bactericidal concentration, MBC)도 시험할 수 있다.
최근 임상 미생물 검사실에서 사용하는 자동화 장비는 액체 배지 미량 희석 법으로 MIC를 측정한다.
한천 희석 법은 많은 균주에 대한 MIC를 측정할 때 많이 쓰이고, 액체 배지 희석 법보다 편리하고 재현성이 높다.
또, 오염이나 감수성의 다른 소수의 변이 세균이 섞이는 것으로 나타났다.
3. 3. E-testEtest는 희석 법과 확산 법의 결합이라고 말할 수 있어 각각 분리된 MIC값에 의해서 항생제 감수성을 직접 측정할 수 있다.
디스크 확산 법과 같은 방법으로 검사 하지만 전통적인 디스크 확산 법과는 개념적인 차이를 보인다.
항 상제의 농도 경사는 미리 형성되어 결정됐고 안정적으로 확산에 의존하지 않는다.
Etest은 가로 5mm, 세로 60mm의 길고 비활성 또는 삼투성의 플라스틱 스트립이다.
이 스트립 윗면에는 MIC(μg/mL)눈금이 인쇄되어 있으며 상부에는 2자릿수의 항생제 코드가 나타나고 있다.
접종된 배지 위에 Etest스트립을 싣고 배양하면 스트립에 따라서 좌우 대칭형 억제대가 나타나고 이 억제대와 스트립이 만나는 점을 MIC값에서 판독한다.
항바이러스성 평가바이러스 정량은 바이러스 백신 바이러스 항원을 사용하는 조환에 단백질, 항 바이러스제 연구 또는 생산 생산 수율을 최적화하고 끊임없이 변화하는 요구와 응용에 대응하기 위해서 꼭 필요하다.
바이러스를 정량화하기 위한 가장 일반적으로 쓰이는 방법은 플라크 분석, 50%조직 배양 감염 용량(TCID50), 형광 초점 분석(FFA)이 있다.
1. 페스트 분석(Plaque Assay)플라크(plaque)는 바이러스 감염에 의해서 세포 변성을 일으킨 단층 세포 부위에서 플라크 주위의 감염되지 않은 정상 세포는 vital dye에 염색되므로 구별된다.
각 세균별로 특징적인 집 라크가 만들 수 있도록 각 바이러스마다 크기와 모양이 다른 특징적인 플라크가 생성된다.
하나의 감염성이 있는 바이러스 입자는 하나의 플라크를 형성한다는 이론 아래 plaque assay는 각종 바이러스의 정량에 사용된다.
plaque assay는 CPE을 나타내는 바이러스의 정량에만 사용할 수 있다.
세포 단층을 마련한 후 정량하려는 바이러스 부유 액을 10배수 희석해서 접종한다.
1-2시간 정도 바이러스를 흡착시킨 뒤 overlaymedia를 가하다.
overlaymedia는 영양을 공급하는 동시에 최초의 감염 세포에서 증식한 바이러스가 배지를 통해서 돌아 주변 세포를 이차 감염되는 것을 방지하는 역할을 한다.
플라크는 바이러스에 감염되어 있지 못하는 주변 건강한 세포 단층과 대조되어 무색의 명확한 foci로 나타난다.
Plaque counting을 더 쉽도록 vital dye으로 세포에 단층을 염색하기도 한다.
플라크 수를 세며 접종량과 희석 배수를 감안하여 바이러스 stock의 titer는 plaque forming units per milliliter(PFU/mL)에서 나타낸다.
2. 형광초점분석 (Fluorescent-Focus Assay, FFA)Fluorescent-Focus Assay(FFA)은 plaque assay의 변형으로 세포를 죽이지 않거나 CPE가 명확하지 않은 바이러스의 정량에 이용된다.
세포 단층 마련, 바이러스 접종 overlaymedia첨가 등의 과정은 같지만 육안으로 볼 수 있는 세포 변화가 없고 일정 기간 후에 methanol또는 aceton으로 세포에 단층을 고정시킨 뒤 면역 형광 염색을 시행한다.
형광 현미경 아래 fluorescent foci를 계산하고 plaque assay 같은 방식으로 fluorescent-focus-forming unit per milliliter(FFU/mL)를 측정한다.
3. 종말 점 희석 분석 법(Tissue culture infective dose 50, TCID50)50%조직 배양 감염 용량(TCID50)은 감염성 바이러스 역치의 척도이다.
이 종말 점 희석 분석은 감염된 숙주 50%를 사멸시키거나 접종된 배양 세포의 50%에서 세포 변성 효과(cytopathiceffect, CPE)을 생성하는 데 필요한 바이러스의 양을 정량화한다.
이 분석은 치명적인 용량의 바이러스를 결정하거나 바이러스 플라크를 형성하지 않는 임상 연구 분야에서 더 일반적으로 될 수 있다.
10배수별로 바이러스를 접종한 세포 단층을 관찰하고 CPE의 유무를 판정하고 감염된 well의%를 계산한다.
TCID50분석은 일반적으로 세포 배양에서 감염을 확립하는데 요구되는 시간은 최대 7일 정도 걸린다.
플루오레스센트-포커스 어세이(FFA)는 plaque assay 변형으로 세포를 죽이지 못하거나 CPE가 명확하지 않은 바이러스 정량에 이용된다.
세포단층 만들기, 바이러스 접종, 오버레이미디어 첨가 등의 과정은 동일하지만 육안으로 볼 수 있는 세포 변화가 없기 때문에 일정 기간 후 메타놀 또는 aceton으로 세포단층을 고정시킨 후 면역형광염색을 시행한다.
형광현미경 아래에서 fluorescent foci를 계산하여 plaque assay와 같은 방식으로 fluorescent-focus-forming unit per milliter(FFU/mL)를 측정한다.
3. 종말점 희석분석법(Tissue culture infective dose 50, TCID 50) 50% 조직배양감염용량(TCID 50)은 감염성 바이러스 역치 척도다.
이 종말점 희석 분석은 감염된 숙주의 50%를 사멸시키거나 접종된 배양세포의 50%에서 세포변성 효과(cytopathiceffect, CPE)를 생성하는 데 필요한 바이러스의 양을 정량화한다.
이 분석은 치명적 용량의 바이러스를 결정하거나 바이러스가 플라크를 형성하지 않는 임상 연구 분야에서 더 일반적일 수 있다.
10배수별로 바이러스를 접종시킨 세포단층을 관찰하고 CPE 여부를 판정해 감염된 웰의 %를 계산한다.
TCID50 분석은 일반적으로 세포 배양으로 감염을 확립하는 데 요구되는 시간은 최대 7일 정도 걸린다.
※항 바이러스 능력 평가시의 주요 고려 사항※전술처럼 바이러스는 단백질과 핵산(DNA나 RNA 같은 유전 물질)로 이루어진 생물과 무생물의 중간 형태의 미생물로 스스로 물질 대사가 없다.
그래서 동식물과 미생물의 살아 있는 세포에 기생하는 세포 내 침투한 바이러스는 핵산을 이용하고 자신을 무수하게 복제하면서 증식한다.
즉, 항 바이러스 평가를 하려면 바이러스의 생장 및 관찰에 필수적인 “세포 배양”이 기본 조건이다.
만약 세포의 활성이 떨어지거나 항 바이러스 능력을 평가하는 제품이 host세포에 독성을 가지고 있으면 세포는 정상적인 성장을 못하고 그 결과 바이러스 평가도 안 되는 것이다.
정확한 항 바이러스성 분석을 위해서는 분석하려는 제품이 세포에 대해서 독성이 없는지 확인하는 MTTassay(세포 독성 조사)을 선행으로 진행하고 해당 농도의 제품을 사용하고 항 바이러스성 분석을 진행시키는 것이 가장 이상적이다.
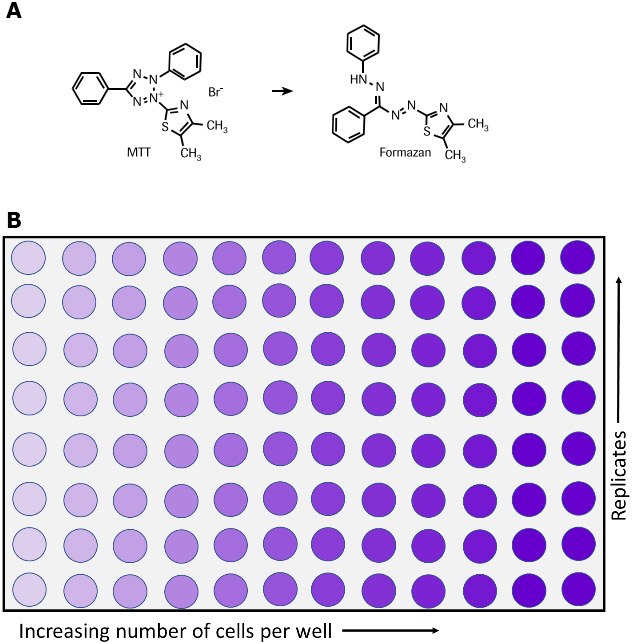
<MTTassay방법>MTTassay는 세포 독성도 조사라는 어느 화합물(또는 물질)이 세포에 어느 정도 독성을 나타내는지 확인하는 실험이다.
MTTassay는 이미 작품의 미토콘드리아의 활성을 측정하는 실험이지만 미토콘드리아는 세포 내에 에너지를 공급하는 기관이다.
그러므로 미토콘드리아가 파괴되면 ATP가 생성되지 않아 세포가 죽게 되고 이를 분석하는 원리이다.
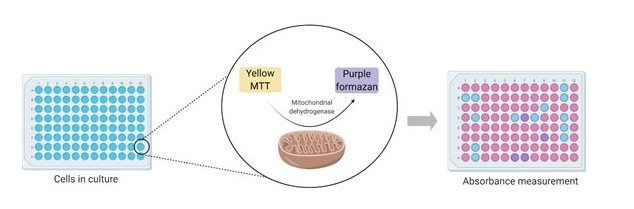
살아 있는 세포에 MTT를 처리하면 MTT이 미토콘드리아에 있는 reductase에 의해서 환원되고 formazan으로 불리는 crystal을 형성하게 된다.
죽은 세포에서는 미토콘드리아가 이미 깨지지 않아 reductase도 존재하지 않고 formazan이 형성되지 않기 때문에 비교가 가능하다.
시료 화합물을 농도 기울기 따로 formazan의 형성을 측정하면 약 50%정도 세포가 살아 있는 농도를 결정할 수 있지만, 이 값을 IC50이라 부르며 IC50값은 화합물별로 다르기 때문에 그 화합물의 고유의 특성이나 된다.
한국의 과학 연구원 미생물 분석 센터는 국내 유수 기관의 항균 능력, 살균 능력, 항 바이러스 방사능에 대한 평가하고 있다.
또 실험을 통해서 얻은 항생제 내성 세균과 이와 관련된 실험 정보 빅 데이터를 수집하고 항생제 내성 세균 발생 메카니즘과 진화 등의 기초 연구, 항생제 내성 발생 방지를 위한 연구, 신약 대체제 개발 등의 연구 발전에 기여하고 있다.
유해 미생물에 저항하는 항균 능력은 시시각각 변화하는 환경과 돌연변이로 나타나는 건강을 위한 바이러스가 출몰하는 현대에 우리의 일상의 모든 제품과 물질에 대한 항 바이러스 및 항균 능력의 관점의 연구가 큰 관심을 끌고 있다.
한의과학연구원 미생물분석센터는 국내 유수기관의 항균능, 살균능, 항바이러스능에 대한 평가를 진행하고 있다.
또한 실험을 통해 얻은 항생제 내성 세균과 이와 관련된 실험정보 빅데이터를 수집하여 항생제 내성 세균 발생 메커니즘과 진화 등 기초연구, 항생제 내성 발생 방지를 위한 연구, 신약 대체제 개발 등의 연구발전에 기여하고 있다.
유해 미생물에 저항하는 항균능은 시시각각 변화하는 환경과 돌연변이로 나타나는 건강을 위한 바이러스가 출몰하는 현대에 우리 일상의 모든 제품과 물질에 대한 항바이러스 및 항균능 관점의 연구가 큰 관심을 끌고 있다.
한국의 과학 연구원 한국의 과학 연구, 마이크로 바이옴 연구, 미생물 자원 연구, NGS분석, 장내 미생물 분석, 장내 세균 분석(GMA), Korean Gut Microbiome Project, 산학연 공동 연구, 미생물 분석, 임상 평가 및 인증 평가 및 시험 성적 발행 www.okkr.kr한의과학연구원 한의과학연구, 마이크로바이옴연구, 미생물자원연구, NGS분석, 장내미생물분석, 장내세균분석(GMA), Korean Gut Microbiome Project, 산학연공동연구, 미생물분석 , 임상평가 및 인증 , 평가 및 시험성적발행 www.okkr.kr한의과학연구원 한의과학연구, 마이크로바이옴연구, 미생물자원연구, NGS분석, 장내미생물분석, 장내세균분석(GMA), Korean Gut Microbiome Project, 산학연공동연구, 미생물분석 , 임상평가 및 인증 , 평가 및 시험성적발행 www.okkr.kr
.png?type=w800)